 Odkąd istotnym elementem życia dla konsumentów stał się młody, atrakcyjny wygląd i dobre samopoczucie, trwają poszukiwania eliksiru młodości. Naukowcy włożyli wiele sił i nakładów na coraz bardziej szczegółowe badanie przyczyn procesów starzenia się, mechanizmów oraz związków, które miałyby korzystny wpływ na ich spowolnienie. Dzięki wieloletnim badaniom lekarze i kosmetolodzy dysponują dziś licznymi metodami „odmładzającymi”.
Odkąd istotnym elementem życia dla konsumentów stał się młody, atrakcyjny wygląd i dobre samopoczucie, trwają poszukiwania eliksiru młodości. Naukowcy włożyli wiele sił i nakładów na coraz bardziej szczegółowe badanie przyczyn procesów starzenia się, mechanizmów oraz związków, które miałyby korzystny wpływ na ich spowolnienie. Dzięki wieloletnim badaniom lekarze i kosmetolodzy dysponują dziś licznymi metodami „odmładzającymi”.
Jak wskazują najnowsze badania, starzenie nie jest tylko wynikiem zmian zależnych od czynników genetycznych i środowiskowych, ale również modyfikacji epigenetycznych. Z uwagi na fakt, że naukowcy prowadzą badania nad możliwością odwrócenia działania zegara biologicznego przez tzw. reprogramowanie epigenetyczne komórek oraz udział w tych procesach, m.in.: enzymów sirtuin, istotne stało się zrozumienie, jak białka SIRT (sirtuiny) mogą wpływaćna procesy starzenia, odmładzania oraz regeneracji.
Poszukiwane są substancje, które w znaczący sposób mogłyby regulować działanie sirtuin, dając wymierne i oczekiwane korzyści (hamujące lub pobudzające). Liczne badania zaowocowały opracowaniem związków, które mogłyby regulować działanie „enzymów długowieczności”. Na rynku pojawiły się produkty nowej generacji zawierające tzw. modulatory sirtuin.
Sirtuiny – charakterystyka
Już w starożytności poszukiwano eliksiru młodości. Jedno z największych odkryć naukowców jako geny długowieczności wskazuje te o symbolach: p66shc, ink4a, daf-2, sir-2. Ten ostatni koduje powstawanie sirtuin – białek nazywanych eliksirem nieśmiertelności. Rzeczywiście wykazano, że poziom sirtuin reguluje długość życia wielu organizmów, od drożdży, poprzez muszki, aż po naczelne.
Sirtuiny (białka SIRT, białka Sir2 – nazywane tak z uwagi na to, że są produktami genów Sir2) należą do grupy enzymów – deacetylaz histonowych – HDAC (histone deacetylase). Niektóre enzymy wymagają obecności pewnych kofaktorów do pełnienia swojej funkcji katalitycznej. Wyróżnia się trzy klasy HDAC, z których dwie pierwsze wykorzystują jako kofaktor cynk, natomiast trzecia klasa, którą stanowią sirtuiny, to enzymy, których aktywność jest zależna od dinukleotydu nikotynoamidoadeninowego (NAD+).
Sirtuiny to ewolucyjnie konserwowane enzymy, których występowanie stwierdzono u wszystkich zbadanych organizmów eukariotycznych i wielu prokariotycznych. W organizmach ssaków zidentyfikowano siedem homologów tych enzymów (SIRT 1-7). Jedna z klasyfikacji ich podziału opiera się na miejscu występowania poszczególnych z nich. Wyróżnia się sirtuiny występujące głównie w jądrze komórkowym (SIRT1, 6 i 7), w mitochondrium (SIRT3, 4 i 5) oraz w cytoplaźmie – SIRT2. Sirtuiny charakteryzują się podwójną aktywnością metaboliczną: deacetylacją (czyli odszczepianiem reszty kwasu octowego od białkowych substratów) oraz ADP-rybozylacją, obie sprzężone z hydrolizą NAD+. Dzięki temu mogą odpowiadać za regulację wielu procesów biologicznych. Ogólną charakterystykę sirtuin wraz z ich substratami i biologiczną funkcją przedstawiono w tabeli 1.
Tabela 1 Ogólna charakterystyka sirtuin
| Sirtuiny |
Lokalizacja |
Aktywność |
Substrat |
Biologiczna funkcja |
| SIRT1 |
Jądro komórkowe |
Deacetylacja |
PGC-1α, FOXOs,
p53, NF-κB |
Udział w procesach metabolicznych,
zapalnych |
| SIRT2 |
Cytoplazma |
Deacetylacja |
α-tubulina |
Kontrola cyklu komórkowego |
| SIRT3 |
Mitochondrium |
Deacetylacja |
AceCS |
Udział w procesach metabolicznych |
| SIRT4 |
Mitochondrium |
ADP-rybozylacja |
Dehydrogenaza
glutaminianowa |
Kontrola sekrecji isnuliny |
| SIRT5 |
Mitochondrium |
Deacetylacja |
Cytochrom c |
Kontrola procesów metabolicznych (?) |
| SIRT6 |
Jądro komórkowe |
ADP-rybozylacja |
Polimeraza DNA |
Naprawa DNA |
| SIRT7 |
Jądro komórkowe |
Nieokreślona |
Polimeraza RNA I |
Transkrypcja rDNA |
PGC-1α – koaktywator-1α receptora gamma aktywującego proliferację peroksysomów, FOXOs – czynnik transkrypcyjny
O z rodziny forkhead, NF-κB – jądrowy czynnik transkrypcyjny B, AceCS – syntetaza acetyloCoA
Działanie regulatorowe sirtuin na różne procesy metaboliczne jest możliwe dzięki dużej specyficzności substratowej i oddziaływaniu na liczne substraty w ogóle.
Najlepiej poznaną sirtuiną jest SIRT1. Dotychczasowe badania wskazują na jej zdolność do modulowania aktywności m.in. takich białek, jak p53 czy czynnik transkrypcyjny O z rodziny forkhead (FOXO). Deacetylacja białka p53 przez SIRT1 powoduje jego inhibicję, co ingeruje w proces apoptozy, czyli programowanej śmierci komórki, wydłużając jej przeżycie. Czynniki transkrypcyjne z rodziny FOXOs uczestniczą w regulacji procesów komórkowych, jak różnicowanie, metabolizm, proliferacja,
promowanie ich przeżycia, nasilanie procesów naprawczych DNA i obrony antyoksydacyjnej.
 SIRT6 bierze udział w procesie naprawy uszkodzonych nici DNA poprzez m.in. aktywację BER (base excision repair), czyli wycinanie wadliwych zasad tworzących nić DNA, modyfikacje chromatyny prowadzące do łatwiejszego wiązania się z czynnikami transkrypcyjnymi oraz poprzez regulowanie procesów zmniejszających ilość wytwarzania reaktywnych form tlenu ROS (reactive oxygen species). Wpływ na regulację odpowiedzi komórek na stres oksydacyjny ma również cytoplazmatyczna
SIRT6 bierze udział w procesie naprawy uszkodzonych nici DNA poprzez m.in. aktywację BER (base excision repair), czyli wycinanie wadliwych zasad tworzących nić DNA, modyfikacje chromatyny prowadzące do łatwiejszego wiązania się z czynnikami transkrypcyjnymi oraz poprzez regulowanie procesów zmniejszających ilość wytwarzania reaktywnych form tlenu ROS (reactive oxygen species). Wpływ na regulację odpowiedzi komórek na stres oksydacyjny ma również cytoplazmatyczna
SIRT2, ponieważ deacetylując czynnik FOXO3, wpływa na ekspresję docelowych genów kodujących takie białka, jak: p27, MnSOD, Bim. Białko p27 bierze udział w kontrolowaniu prawidłowej proliferacji komórki i w apoptozie. MnSOD jest zaangażowany w walkę z wolnymi rodnikami i reaktywnymi formami tlenu w trakcie procesów patologicznych, a Bim to białko proapoptotyczne, biorące udział w indukcji tego procesu szczególnie w przypadku w odpowiedzi na stres komórkowy (np. hipoksja, infekcje, wzrost stężenia białek onkogennych, niewystarczający poziom cytokin).
SIRT3 odpowiada za deacetylację histonów, białek strukturalnych, jak: tubulina czy białek z rodziny FOXOs. Reguluje też aktywność innego enzymu – syntetazy acetyloCoA, uczestniczącego w syntezie acetylo-CoA. Związek ten jest wykorzystywany w wielu szlakach metabolicznych, np.: wytwarzania energii w cyklu kwasów trikarboksylowych, syntezie cholesterolu czy biosyntezie kwasów tłuszczowych, z których zbudowane są między innymi błony komórkowe. Głównym substratem dla SIRT4 jest dehydrogenaza glutaminianowa, biorąca udział w utrzymaniu homeostazy glukozy, między innymi poprzez stymulację sekrecji insuliny. SIRT5 jest jeszcze stosunkowo słabo poznana i wydaje się, że bierze udział w procesie oddychania komórkowego
i tzw. wewnętrznym szlaku apoptozy.
Zasadniczo wykazano, że sirtuiny mają swój udział w: regulacji transkrypcji, naprawy DNA, utrzymywania stabilności chromosomów, modyfikacji potranslacyjnej białek, mechanizmów kompensacyjnych uruchamianych w odpowiedzi na niekorzystne warunki, apoptozy, karcenogenezy, regulacji procesów metabolicznych, wyciszania genów czy opóźniania starzenia komórek, wydłużania cyklu replikacyjnego (życia komórek i organizmów) i wielu innych. Mają one znaczenie m.in. dla specjalizacji związanych z pielęgnacją czy leczeniem, m.in. skóry, ponieważ białka te stanowią klucz do wielu szlaków komórkowych związanych z chorobami skóry.
Sirtuiny odgrywają rolę w starzeniu skóry, zapaleniu skóry, łuszczycy i innych chorobach skóry z hiperproliferacją, chorobach autoimmunologicznych, takich jak toczeń rumieniowaty układowy SLE (systemic lupus erythematosus), infekcjach grzybiczych skóry, dziedzicznych chorobach dermatologicznych czy raku skóry. Poznanie ich mechanizmu działania, wywieranych wpływów i oddziaływań z różnego typu modulatorami – aktywatorami i inhibitorami, nieustanne poszerzanie wiedzy na ten temat, niesie ogromne nadzieje na leczenie wielu schorzeń (nie tylko skórnych), poprawy jakości życia w parze z dobrym wyglądem i kondycją.
Modyfikacje epigenetyczne
Epigenetyka oznacza dziedziczne zmiany w organizacji chromatyny i ekspresji genów, które nie są zakodowane w sekwencji genów. Wszystkie komórki organizmu mają ten sam zestaw informacji genetycznej w postaci DNA. Jednak ekpresjonowane (aktywne) geny w każdej z nich w danym momencie mogą być różne, w zależności od zapotrzebowania, tkanki. Jest to możliwe m.in. dzięki modyfikacjom epigenetycznym, takim jak metylacja i acetylacja. Zmiany w ekspresji genów są wywoływane przez szeroko rozumiane sygnały z otoczenia, w tym przez bioaktywne składniki diety czy aplikowane na skórę produkty.
O stopniu aktywności transkrypcyjnej genu decyduje poziom metylacji DNA oraz modyfikacje białek histonowych wchodzących w skład chromatyny. Metylacji podlega około 75% reszt cytozyny występującej w dinukleotydowych sekwencjach CpG. Tkankowo specyficzna metylacja następuje już podczas embriogenezy na etapie blastocysty, dlatego w tym okresie dieta matki bogata w kwas foliowy jako źródło donoru grupy metylowej i warunki środowiskowe mają znaczny wpływ na profil metylacji DNA u dziecka. Zaburzenia tego procesu mogą prowadzić do utrwalenia nieprawidłowego profilu metylacji DNA. Nieprawidłowości takie polegają na hipermetylacji lub hipometylacji sekwencji CpG. Hipermetylacja prowadzi do represji transkrypcji,
natomiast hipometylacja wywołuje aktywację transkrypcji tych genów, które powinny pozostać wyciszone.
Profil metylacji DNA zmienia się pod wpływem diety, polimorfizmów pojedynczego nukleotydu w określonych genach oraz ekspozycji na czynniki środowiskowe. Niedobory np.: kwasu foliowego, metioniny lub selenu mogą powodować hipometylację DNA, co z kolei może prowadzić do niewłaściwej ekspresji genów oraz niestabilności genetycznej. Nieprawidłowy profil modyfikacji DNA oraz histonów może być przyczyną wielu chorób, począwszy od chorób nowotworowych, przez metaboliczne, a kończąc na chorobach neurodegeneracyjnych. Dowiedziono, że podobne zmiany jak w komórkach starych obserwowane są także w komórkach nowotworowych, gdzie spadek metylacji DNA powoduje niestabilność materiału genetycznego, wzrostu liczby mutacji, co może inicjować karcenogenezę. Zainteresowanie epigenetyczną regulacją transkrypcji wynika nie tylko z przyczyn poznawczych, ale także z poszukiwania nowych rodzajów terapii. Tym bardziej że inaktywacja niektórych genów w wyniku zmian epigenetycznych jest procesem odwracalnym.
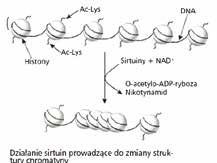
Jedynie niektóre geny ulegają stałej ekspresji. Są to tzw. housekeeping genes, warunkujące podstawowe funkcje życiowe. Transkrypcja pozostałych genów jest regulowana m.in. na drodze acetylacji i deacetylacji białek histonowych oraz metylacji DNA. Oba mechanizmy wpływają na strukturę chromatyny (rys. 1). Zmetylowane cytozyny (jedna z zasad azotowych budujących DNA) są rozpoznawane przez grupę białek (MBDs) wiążących odpowiednie deacetylazy. Następująca w tym miejscu deacetylacja histonów powoduje utworzenie się zbitej, nieaktywnej struktury chromatyny. Zmetylowanie nukleotydu uniemożliwia także przyłączenie się do niego czynników transkrypcyjnych. Taka modyfikacja zmniejsza również ekspresję genów wirusowych i innych szkodliwych elementów włączonych do genomu gospodarza.
Białka histonowe leżą u podstaw wielu procesów dziedziczenia epigenetycznego. Mogą one ulegać modyfikacjom posttranslacyjnym, polegającym na przyłączeniu różnych dodatkowych cząsteczek lub grup funkcyjnych (takich jak grupa metylowa, acetylowa, fosforanowa, białko ubikwityna) do aminokwasów: lizyny i argininy. Modyfikacje takie mogą być sygnałem dla białek przebudowujących chromatynę. Chromatyna może być kondensowana (heterochromatynizacja) w miejscu, gdzie występuje taka modyfikacja, co zatrzymuje ekspresję genów. Przykładem może być metylacja histonu H3 na dziewiątym aminokwasie (lizyna), która u wielu organizmów powoduje zmniejszenie ekspresji genów. Znane są modyfikacje histonów prowadzące do rozluźnienia struktury chromatyny i zwiększenia poziomu ekspresji genów. Warto zauważyć, że wpływ modyfikacji posttranslacyjnych histonów na stopień kondensacji chromatyny i ekspresję genów nie zależy tylko od rodzaju modyfikacji (metylacja, acetylacja, fosforylacja itp.), ale także od miejsca wystąpienia takiej modyfikacji na białku histonowym. Metylacja lizyny 9 histonu H3 może wywoływać zupełnie inny efekt niż metylacja lizyny 4. Jedna cząsteczka histonu może być modyfikowana w wielu miejscach. Istotne znaczenie epigenetyki w starzeniu się organizmów oraz w procesie starzenia komórkowego potwierdzają również badania dotyczące białek z rodziny sirtuin. SIRT deacetylują m.in. histony, głównie H3 i H4 (reszty lizyny w obrębie N-terminalnych domen histonów). Wpływa to na zwiększenie stopnia pofałdowania tych białek, które przyjmują bardziej zwartą strukturę. Następstwem tego staje się bardziej zbita struktura chromatyny, regionalnie niedostępna dla aparatu
transkrypcyjnego, przez co mogą wpływać na hamowanie ekspresji różnych genów.
 Wspomniane reprogramowanie epigenetyczne jest definiowane jako proces modyfikacji aktywności genów, pozwalający na cofnięcie komórek do wcześniejszego etapu rozwoju. Polega na modyfikacji tzw. epigenomu – zestawu cząsteczek związków chemicznych (np. grup metylowych) „przyczepionych” do nici DNA i zmieniających aktywność poszczególnych genów. Reprogramowanie („wyczyszczenie” tych zmian nakumulowanych w genomie w miarę rozwoju organizmu, a także pod wpływem czynników środowiskowych, np. toksyn) sprawia, że jądro znów zaczyna działać jak na wcześniejszym etapie rozwoju, np. pluripotencjalnej komórki macierzystej. Reprogramowanie jest zatem związane z takim regulowaniem substancji biorących udział w modyfikacjach epigenetycznych, by możliwe stało się wpływanie w ukierunkowany i kontrolowany sposób na różne procesy biologiczne. W przypadku elementu eliksiru długowieczności, za jaki uważane są sirtuiny, taki scenariusz samoodmładzania się komórek już wydaje się możliwy. Przynajmniej częściowo i lokalnie, zgodnie z dzisiejszą wiedzą na ten temat.
Wspomniane reprogramowanie epigenetyczne jest definiowane jako proces modyfikacji aktywności genów, pozwalający na cofnięcie komórek do wcześniejszego etapu rozwoju. Polega na modyfikacji tzw. epigenomu – zestawu cząsteczek związków chemicznych (np. grup metylowych) „przyczepionych” do nici DNA i zmieniających aktywność poszczególnych genów. Reprogramowanie („wyczyszczenie” tych zmian nakumulowanych w genomie w miarę rozwoju organizmu, a także pod wpływem czynników środowiskowych, np. toksyn) sprawia, że jądro znów zaczyna działać jak na wcześniejszym etapie rozwoju, np. pluripotencjalnej komórki macierzystej. Reprogramowanie jest zatem związane z takim regulowaniem substancji biorących udział w modyfikacjach epigenetycznych, by możliwe stało się wpływanie w ukierunkowany i kontrolowany sposób na różne procesy biologiczne. W przypadku elementu eliksiru długowieczności, za jaki uważane są sirtuiny, taki scenariusz samoodmładzania się komórek już wydaje się możliwy. Przynajmniej częściowo i lokalnie, zgodnie z dzisiejszą wiedzą na ten temat.
Modulowanie aktywności sirtuin
Z licznych badań naukowych wynika, że poza wieloma procesami zależnymi od sirtuin, warunkującymi homeostazę i prawidłowe funkcjonowanie organizmu, stanowią one element stabilnego ewolucyjnie mechanizmu genetycznej kontroli starzenia, uruchamianego i promującego przeżycie organizmów w niekorzystnych warunkach środowiska. Sirtuiny są aktywne, dopóki komórki skóry są młode. Wtedy proces podziałów komórkowych odbywa się prawidłowo, a tworzenie nowych i zamieranie starszych komórek pozostaje w równowadze.
Z biegiem lat pojawia się chronostarzenie pod wpływem czynników zewnętrznych i wewnętrznych, podziały komórkowe zaczynają zwalniać. Cera zaczyna wyglądać na zmęczoną, traci jędrność, pojawiają się zmarszczki. Mobilizowanie sirtuin do aktywności opóźnia niekorzystne zmiany w strukturach włókien kolagenu i elastyny, zapewnia silne działanie ochronne wobec wolnych rodników. A nic tak nie utrzymuje gładkiej skóry, jak dobrze uporządkowana warstwa kolagenowo-elastynowa skóry właściwej, dobre nawilżenie i zdolność skóry do walki z wolnymi rodnikami. Pobudzone sirtuiny działają na fibroblasty odpowiedzialne za wytwarzanie białek budulcowych kolagenu i elastyny w skórze właściwej, jak i keratynocytów tworzących naskórek. Dzięki temu działanie przeciwstarzeniowe i przeciwzmarszczkowe dotyczy nie tylko powierzchniowej, ale i głębszej warstwy skóry. Zadaniem preparatów z modulatorami sirtuin jest przypominanie dojrzałemu naskórkowi, jak powinien działać.
Jak zatem zmusić organizm czy poszczególne typy komórek do produkcji sirtuin?
Gen sir-2 jest m.in. pobudzany przez enzymy, które zwykle zajmują się przetwarzaniem glukozy. Gdy w organizmie jest jej za mało, w wyniku np. niskokalorycznej diety, enzymy te „z nudy” przenoszą swoją aktywność na stymulowanie genu długowieczności. To właśnie dlatego niskokaloryczna dieta wydłuża życie.
Liczne badania tej grupy białek wykazują, dlaczego ludzie oraz zwierzęta żyją dłużej i są zdrowsze, gdy dostarczają swoim organizmom mniej kalorii. Podczas tzw. restrykcji kalorycznej (krótkotrwałej u ludzi i długotrwałej u zwierząt) zwiększa się ekspresja genów Sirt, których produktami są białka – sirtuiny (SIRT). Ich aktywność wywołuje zmiany w kondensacji chromatyny, a co za tym idzie – zmiany w ekspresji różnych genów. Uruchamiany jest inny mechanizm działania komórek nastawiony na przetrwanie w trudnych warunkach. Priorytetem staje się naprawa uszkodzeń, regeneracja, zmienia się intensywność metabolizmu, funkcjonowanie układu hormonalnego i ekspresja genów. Połączenie tych wszystkich zmian w konsekwencji
wpływa na opóźnienie starzenia. Zatem pierwszym i podstawowym modulatorem enzymów długowieczności jest dieta – restrykcja kaloryczna CR (caloric restriction).
Poza ograniczeniem podaży kalorii w diecie, potwierdzono naukowo, że niektóre substancje mają zdolność do stymulacji wzrostu poziomu enzymów długowieczności „peptydów głodu” oraz pozytywnie wpływają na ich aktywność manifestowaną zewnętrznie jako przedłużanie życia komórek, poprawę ich działania, regenerację, hamowanie apoptozy lub jej indukowanie w komórkach nowotworowych. Odnosi się to nie tylko do komórek skóry, ale całego organizmu (dlatego m.in. sirtuiny stały się ostatnimi czasy obiecującym celem badań zarówno w opóźnianiu procesu starzenia, jak i poprawy jakości życia ludzi starszych czy leczeniu różnych schorzeń, szczególnie ujawniających się w późniejszym wieku). Takie substancje czy działania nazywane są często modulatorami sirtuin (aktywatorami oraz inhibitorami).
Liczność badań i wniosków patentowych wskazuje na ważność tych białek w leczeniu różnych schorzeń. Często można odnieść wrażenie, że wpływ na proces odmładzania, spowolnienie starzenia to tylko wspaniały efekt uboczny stosowania leków na różne schorzenia, działający od wewnątrz. Wielu naukowców, bazując na syntetycznych pochodnych resweratrolu, działających silniej niż pierwowzór, np.: SRT1720, SRT1460, SRT2183, uzyskało bardzo obiecujące rezultaty dla leków na otyłość oraz prowadzącą do cukrzycy opornością na insulinę. Inni, badając ten sam lek pod kątem długowieczności, otrzymali wyniki wydłużenia średniej długości życia gryzoni o 8,8%!!!
W kosmetologii najbardziej znanym i najczęściej stosowanym aktywatorem sirtuin jest sam resweratrol – polifenol pochodzenia roślinnego (3,5,4’-trihydroksystilben), który rośliny wytwarzają w obronie przed infekcjami. Zwiększa aktywność ludzkiej sirtuiny SIRT1 in vitro około 13-krotnie. Występuje w dwóch postaciach chemicznych: cis i trans. Tylko forma trans jest aktywna biologicznie. Jednak może przejść w nieaktywną biologicznie formę cis pod wpływem promieniowania UV. Resweratrol zawarty jest przedewszystkim w winogronach (głównie skórkach), czerwonym winie (produkty z odpowiednimi wyciągami są czasami określane jako „Wine Therapy”), orzeszkach ziemnych, w skórce owoców, jak morwa czy czarna porzeczka.
Również monakolina K – fitostatyna pochodząca z czerwonego ryżu poddanego fermentacji przez grzyby Monascuc purpureus, jest w stanie aktywować SIRT1. Co więcej, aktywuje ona ścieżkę SIRT1/AMPK/FOXO1, w wyniku czego zmniejsza poziom lipidów przez hamowanie syntazy kwasów tłuszczowych (FAS, ang. fatty acid synthase).
Właściwości aktywowania sirtuin wykazano również dla: ekstraktów z mirtu (Myrtus communis), kawioru, ryżu siewnego (Oryza sativa), pimenty lekarskiej (Pimenta officinalis) oraz orsirtine – ekstraktu z ryżu bogatego w peptydy i dla biopeptydów otrzymywanych ze szczepu drożdży.
Zdolność sirtuin do regulacji gospodarki lipidowo-węglowodanowej i uruchamiania mechanizmów naprawczych, a także stymulowanie wzrostu i promowanie przeżycia komórek nadaje tym niewielkim enzymom szczególne znaczenie. Przeprowadzane do tej pory badania na pewno dostarczają ogromnej wiedzy na temat aktywności sirtuin i mechanizmów je regulujących, jednak zdaniem niektórych naukowców, nadal bez odpowiedzi pozostaje wiele pytań, które wymagają intensyfikacji badań nad właściwościami biologicznymi i możliwościami terapeutycznego zastosowania sirtuin.
Niektórzy badacze uważają, że rola sirtuin została przeceniona. Przykładowo, zespół naukowców wykazał, że resweratrol oraz STAC zwiększają produkcję sitruin tylko w obecności fluorescencyjnych markerów użytych w eksperymencie. Mimo że świat nauki zawsze bierze możliwość obalenia tezy w danej tematyce, wydaje się, że ilość badań potwierdzających korzystny wpływ sirtuin na procesy zachodzące w organizmie, liczność tych procesów oraz możliwość regulacji przez różne substancje
naturalne i syntetyczne, skutecznie broni przyjętych teorii i wagi sirtuin jako elementu eliksiru młodości.
Podsumowanie
Wykorzystując wiedzę na temat mechanizmu działania sirtuin – modyfikacje epigenetyczne mogą stanowić cel przyszłych i coraz bardziej zaawansowanych terapii odmładzania, poprawy jakości życia i leczenia chorób. Kluczem do wykorzystania sirtuin w odpowiedniej strategii leczenia jest odpowiednia regulacja działania tych enzymów i ich poziomu w komórkach poprzez ich modulatory (aktywatory i inhibitory).
Dostępne obecnie produkty kosmetyczne nowej generacji zawierające modulatory sirtuin z pewnością mają pozytywny wpływ na jakość i wygląd skóry. Szczególnie że obecne składniki aktywne mają zazwyczaj dodatkowe właściwości antyoksydacyjne, nawilżające i odżywcze oraz są bezpieczne. Niemniej jednak wciąż wydaje się konieczne jeszcze lepsze poznanie samych modyfikacji oraz określenie profilu epigenetycznego komórek starych i młodych, by możliwe stało się postulowane przez naukowców reprogramowanie w kierunku samoodmładzania się komórek. Zwłaszcza że pojawiają się pierwsze publikacje, które dzięki nowocześniejszym metodom, coraz większej wiedzy i jej dostępności próbują weryfikować znane i uznane za pewnik teorie dotyczące mechanizmów działania, substancji aktywujących i hamujących działanie wieloelementowego układu, mającego wpływ na zdrowie i zachowanie młodego wyglądu. Takie próby z pewnością mogą przyczynić się do ostatecznego wyjaśnienia tajemnicy długowieczności, gdzie sirtuiny wydają się niezaprzeczalnie istotnym elementem „eliksiru młodości”.
BIbliografia
1. M. Dudkowska, K. Kucharewicz: Związki pochodzenia naturalnego modulujące starzenie się i śmierć komórek, Postępy Biochemii 60(2), 2014.
2. M. Gertz, et al.: A Molecular Mechanism for Direct Sirtuin Activation by Resveratol, Journal Plos One, 21, 2012.
3. M. Pieszka, M.P. Pietras: Nowe Kierunki w Badaniach Żywieniowych – Nutrigenomika, Rocz. Nauk. Zoot., 2, 2010, 83-103.
4. A.K. Ławniczak: Ocena ekspresji sirtuin 1, 3 i 7 w mięśniu sercowym oraz szkieletowym młodych i starych szczurów w warunkach ograniczonej czasowo diety restrykcyjnej oraz cyklu głodzenie-karmienie, praca doktorska, Gdański Uniwersytet Medyczny, 2014.
5. laboratoria.net: Niezwykle ważne dla Twojego organizmu – sirtuiny, 2013.
6. M. Kucińska, M. Murias: Sirtuiny – droga do długowieczności czy ślepy zaułek?, V Zjazd Polskiego Towarzystwa Onkologii i Hematologii Dziecięcej, Międzyzdroje 2010.
7. https://data.epo.org/publication-server/rest/v1.0/publication-dates/20121010/patents/EP1910384NWB1/document.html.
8. http://mojepanstwo.pl/dane/patenty/248736,tytul-wynalazku-pochodne-imidazo-2-1-b-tiazolu-zwiazki-modulujace-sirtuin.
9. J.M. Villalba, F.J. Alcain: Sirtuin activators and inhibitors, Biofactors, 38(5), 2012.
10. M. Moreau, et al.: Enhancing cell longevity for cosmetic application: a complementary approach, Journal of Drugs in Dermatology 6, 2007.
11. C. Burnet, et al.: Absence of effects of Sir2 overexpression on lifespan in C. elegans and Drosophila, Nature, 477, 2010.
12. K. Siedlecka, W. Bogusławski: Sirtuiny – enzymy długowieczności?, Gerontologia Polska, 3, 2005.
13. J. Wawrzykowski: Znaczenie i zastosowanie dysmutazy ponadtlenkowej, Uniwersytet Przyrodniczy w Lublinie, 2004.
Źródło: http://kosmetologiaestetyczna.com/




















 Odkąd istotnym elementem życia dla konsumentów stał się młody, atrakcyjny wygląd i dobre samopoczucie, trwają poszukiwania eliksiru młodości. Naukowcy włożyli wiele sił i nakładów na coraz bardziej szczegółowe badanie przyczyn procesów starzenia się, mechanizmów oraz związków, które miałyby korzystny wpływ na ich spowolnienie. Dzięki wieloletnim badaniom lekarze i kosmetolodzy dysponują dziś licznymi metodami „odmładzającymi”.
Odkąd istotnym elementem życia dla konsumentów stał się młody, atrakcyjny wygląd i dobre samopoczucie, trwają poszukiwania eliksiru młodości. Naukowcy włożyli wiele sił i nakładów na coraz bardziej szczegółowe badanie przyczyn procesów starzenia się, mechanizmów oraz związków, które miałyby korzystny wpływ na ich spowolnienie. Dzięki wieloletnim badaniom lekarze i kosmetolodzy dysponują dziś licznymi metodami „odmładzającymi”. SIRT6 bierze udział w procesie naprawy uszkodzonych nici DNA poprzez m.in. aktywację BER (base excision repair), czyli wycinanie wadliwych zasad tworzących nić DNA, modyfikacje chromatyny prowadzące do łatwiejszego wiązania się z czynnikami transkrypcyjnymi oraz poprzez regulowanie procesów zmniejszających ilość wytwarzania reaktywnych form tlenu ROS (reactive oxygen species). Wpływ na regulację odpowiedzi komórek na stres oksydacyjny ma również cytoplazmatyczna
SIRT6 bierze udział w procesie naprawy uszkodzonych nici DNA poprzez m.in. aktywację BER (base excision repair), czyli wycinanie wadliwych zasad tworzących nić DNA, modyfikacje chromatyny prowadzące do łatwiejszego wiązania się z czynnikami transkrypcyjnymi oraz poprzez regulowanie procesów zmniejszających ilość wytwarzania reaktywnych form tlenu ROS (reactive oxygen species). Wpływ na regulację odpowiedzi komórek na stres oksydacyjny ma również cytoplazmatyczna Wspomniane reprogramowanie epigenetyczne jest definiowane jako proces modyfikacji aktywności genów, pozwalający na cofnięcie komórek do wcześniejszego etapu rozwoju. Polega na modyfikacji tzw. epigenomu – zestawu cząsteczek związków chemicznych (np. grup metylowych) „przyczepionych” do nici DNA i zmieniających aktywność poszczególnych genów. Reprogramowanie („wyczyszczenie” tych zmian nakumulowanych w genomie w miarę rozwoju organizmu, a także pod wpływem czynników środowiskowych, np. toksyn) sprawia, że jądro znów zaczyna działać jak na wcześniejszym etapie rozwoju, np. pluripotencjalnej komórki macierzystej. Reprogramowanie jest zatem związane z takim regulowaniem substancji biorących udział w modyfikacjach epigenetycznych, by możliwe stało się wpływanie w ukierunkowany i kontrolowany sposób na różne procesy biologiczne. W przypadku elementu eliksiru długowieczności, za jaki uważane są sirtuiny, taki scenariusz samoodmładzania się komórek już wydaje się możliwy. Przynajmniej częściowo i lokalnie, zgodnie z dzisiejszą wiedzą na ten temat.
Wspomniane reprogramowanie epigenetyczne jest definiowane jako proces modyfikacji aktywności genów, pozwalający na cofnięcie komórek do wcześniejszego etapu rozwoju. Polega na modyfikacji tzw. epigenomu – zestawu cząsteczek związków chemicznych (np. grup metylowych) „przyczepionych” do nici DNA i zmieniających aktywność poszczególnych genów. Reprogramowanie („wyczyszczenie” tych zmian nakumulowanych w genomie w miarę rozwoju organizmu, a także pod wpływem czynników środowiskowych, np. toksyn) sprawia, że jądro znów zaczyna działać jak na wcześniejszym etapie rozwoju, np. pluripotencjalnej komórki macierzystej. Reprogramowanie jest zatem związane z takim regulowaniem substancji biorących udział w modyfikacjach epigenetycznych, by możliwe stało się wpływanie w ukierunkowany i kontrolowany sposób na różne procesy biologiczne. W przypadku elementu eliksiru długowieczności, za jaki uważane są sirtuiny, taki scenariusz samoodmładzania się komórek już wydaje się możliwy. Przynajmniej częściowo i lokalnie, zgodnie z dzisiejszą wiedzą na ten temat.