 W październikowym "Journal of Cosmetic Dermatology" ukazały się badania poświęcone temu, jakie cechy decydują o atrakcyjności kobiecych twarzy oraz jakie metody zapobiegania starzeniu się skóry zostały przyjęte lub są rozważane przez francuskie kobiety, aby zminimalizować niekorzystne oddziaływanie upływającego czasu na skórę twarzy. Okazuje się, że za główne wyznaczniki piękna i atrakcyjności ankietowane uznają: naturalny wygląd, pewność siebie oraz atrakcyjną, zadbaną skórę.
W październikowym "Journal of Cosmetic Dermatology" ukazały się badania poświęcone temu, jakie cechy decydują o atrakcyjności kobiecych twarzy oraz jakie metody zapobiegania starzeniu się skóry zostały przyjęte lub są rozważane przez francuskie kobiety, aby zminimalizować niekorzystne oddziaływanie upływającego czasu na skórę twarzy. Okazuje się, że za główne wyznaczniki piękna i atrakcyjności ankietowane uznają: naturalny wygląd, pewność siebie oraz atrakcyjną, zadbaną skórę.
Wśród tysiąca Francuzek w wieku 25 do 70 lat zostało przeprowadzone online badanie ankietowe. Zaskoczeniem nie jest jeden z oczywistych wniosków autorów pracy, że młodsze twarze są uznane za bardziej atrakcyjne, ale interesującym jest wskazanie przez osoby badane, że szczyt piękna i zarazem największej atrakcyjności przypada u kobiet w wieku około 36 lat. Jednocześnie według 92% respondentek, starzejąc się i mając nawet 70 lat, można również być postrzeganym jako osoba piękna.
To właśnie stan skóry (tj. kolor i jej faktura) zostały uznane za wyznacznik młodego, zdrowego wyglądu oraz fizycznej atrakcyjności. Wśród codziennych praktyk i strategii stosowanych w celu utrzymania dobrze wyglądającej skóry oraz młodego wyglądu, Francuski wymieniły:
- prawidłową dietę,
- regularne ćwiczenia,
- picie wody,
- wystarczającą ilość snu,
- codzienną pielęgnację twarzy i ciała (w zdecydowanej większości podały stosowanie produktów nawilżających) oraz równoczesną ochronę przeciwsłoneczną,
- wizyty u fryzjera.
Niezadowolenie z wyglądu?
Jak zaznacza Agnes Ehlinger-Martin, interesującym jest zjawisko, że blisko 80% kobiet czuje się młodszymi i wierzy, że również wygląda młodziej aniżeli wskazuje na to ich wiek chronologiczny. Jednak po osiągnięciu szczytu swojej atrakcyjności, która przypada na wiek około 36 lat, zaczyna się rozwijać i pogłębiać niezadowolenie z własnej fizyczności oraz dostrzeganie oznak upływającego czasu.
To na jakie problemy w odniesieniu do starzejącej się skóry twarzy najczęściej narzekają kobiety zależy od tego ile mają lat. Jak wskazują wyniki francuskich badań opublikowanych w październiku, kobiety w przedziale 25-30 oraz 35-40 lat martwią się przeważnie zmęczonym wyglądem i szarością skóry oraz jej złym nawilżeniem i suchością. Jako dodatkowy problem zaznaczają również cienie pod oczami. Zmarszczki oraz utrata jędrności skóry zauważana jest dopiero w zdecydowanej większości przez osoby po 45 r.ż. a do problemów ponadto dochodzi wówczas zwiotczenie skóry szyi.
Na ratunek… KOSMETOLOGIA? … MEDYCYNA ESTETYCZNA? … CHIRURGIA PLASTYCZNA?
Bardzo dużym zaskoczeniem dla badaczy było stwierdzenie, że jedynie 9% kobiet spośród wszystkich badanych zadeklarowało, że do tej pory korzystało z przynajmniej jednego zabiegu kosmetycznego o minimalnej inwazyjności (toksyna botulinowa, wypełniacze, terapie laserowe, pilingi chemiczne). Kolejne 39% ankietowanych przyznała, że rozważa w przyszłości poddanie się którejś z procedur.
Na podstawie badań opublikowanych w „Journal of Cosmetic Dermatology” do najpopularniejszych zabiegów kosmetycznych o minimalnej inwazyjności we Francji należą pilingi chemiczne – 6% zadeklarowało ich zastosowanie, a 30% z pewnością wybierze tę metodę w przyszłości.
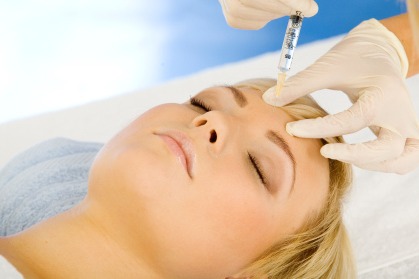 Niespodzianką wydaje się deklarowany negatywny stosunek do procedur z toksyną botulinową wyrażony przez blisko 92% ankietowanych. Zaledwie 1% przyznało, że korzystało z tego zabiegu przynajmniej jeden raz w życiu. Zaskoczenie jest o tyle duże, że według najnowszych doniesień ASAPS (American Society for Aesthetic Plastic Surgery) opublikowanych w odniesieniu do roku 2014 to właśnie toksyna botulinowa (Botox, Dysport, Xaomin) była najchętniej wykorzystywanym zabiegiem z niechirurgicznych procedur kosmetycznych w USA, zostawiając pilingi chemiczne dopiero na czwartym miejscu. Porównując jednak wartości procentowe z 2014 roku w odniesieniu do ilości zabiegów w roku 2013, interesującym w tym kontekście jest fakt, że ilość zabiegów z wykorzystaniem toksyny botulinowej w USA spadła o 4,7%, natomiast ilość procedur z wykorzystaniem pilingów chemicznych wzrosła o 9%.
Niespodzianką wydaje się deklarowany negatywny stosunek do procedur z toksyną botulinową wyrażony przez blisko 92% ankietowanych. Zaledwie 1% przyznało, że korzystało z tego zabiegu przynajmniej jeden raz w życiu. Zaskoczenie jest o tyle duże, że według najnowszych doniesień ASAPS (American Society for Aesthetic Plastic Surgery) opublikowanych w odniesieniu do roku 2014 to właśnie toksyna botulinowa (Botox, Dysport, Xaomin) była najchętniej wykorzystywanym zabiegiem z niechirurgicznych procedur kosmetycznych w USA, zostawiając pilingi chemiczne dopiero na czwartym miejscu. Porównując jednak wartości procentowe z 2014 roku w odniesieniu do ilości zabiegów w roku 2013, interesującym w tym kontekście jest fakt, że ilość zabiegów z wykorzystaniem toksyny botulinowej w USA spadła o 4,7%, natomiast ilość procedur z wykorzystaniem pilingów chemicznych wzrosła o 9%.
Z kolei dla Francuzek zabiegi z obszaru terapii laserowych wydają się być korzystne dla skóry, jednak zbyt drogie i wymagające powtórzeń. Podobny stosunek, jak w przypadku toksyny botulinowej, wykazano w odniesieniu do wypełniaczy skórnych - blisko 90% osób całkowicie odrzuciło możliwość ich stosowania. Analogicznie, w Stanach Zjednoczonych zabiegi z wykorzystaniem kwasu hialuronowego (Juvederm Ultra, Ultra Plus, Voluma, Perlane, Restylane, Belotero) były na drugim miejscu, zaraz za toksyną botulinową. Jednak, tak jak w przypadku toksyny botulinowej, w odniesieniu do 2013 r. wystąpiła i tym razem tendencja spadkowa wynosząca 9,4%.
Ciekawym zjawiskiem, któte widać na podstawie analizy danych pochodzących z ASAPS z lat 1997, 2013 oraz 2014, jest trend dotyczący częstości wykonywania zabiegów chirurgicznych (chirurgia plastyczna) oraz niechirurgicznych (medycyna estetyczna, kosmetologia). W ubiegłym stuleciu, a dokładnie w roku 1997, popularniejsze były zabiegi z zakresu chirurgii plastycznej stanowiące blisko 56% wszystkich wykonanych procedur. W 2013 i 2014 roku zaś 83% zabiegów dotyczyło tych nieinwazyjnych z zakresu kosmetologii oraz medycyny estetycznej, tj. m.in.: z wykorzystaniem wypełniaczy, botoksu, mikrodermabrazji, pilingów czy laserów.
|
Dane dotyczące poszczególnych lat
|
Zabiegi z zakresu chirurgii plastycznej
|
Zabiegi niechirurgiczne (medycyna estetyczna, kosmetologia)
|
Suma wszystkich wykonanych zabiegów (chirurgia plastyczna + medycyna estetyczna + kosmetologia) w danym roku
|
|
N (ilość wykonanych zabiegów w danym roku)
|
Wartość procentowa (%) dla wykonanych zabiegów w danym roku
|
N (ilość wykonanych zabiegów w danym roku)
|
Wartość procentowa (%) dla wykonanych zabiegów w danym roku
|
|
1997
|
939.192
|
55,9%
|
740.761
|
44,1%
|
1.679.943
|
|
2013
|
1.883.048
|
16,5%
|
9.536.562
|
83,5%
|
11.419.610
|
|
2014
|
1.764.956
|
16,6%
|
8.898.652
|
83,4%
|
10.663.607
|
 Tab.1. Tabela opracowana na podstawie danych uzyskanych z raportu ASAPS (American Society for Aesthetic Plastic Surgery) z 2014r.
Tab.1. Tabela opracowana na podstawie danych uzyskanych z raportu ASAPS (American Society for Aesthetic Plastic Surgery) z 2014r.
Jak zauważa w badaniach opublikowanych w 2015 roku Mauro Barone z Uniwersytetu w Rzymie - bardzo często do chirurgów plastycznych trafiają osoby z wyobrażeniem co do ideału urody zaczerpniętym z magazynów modowych, tabloidów, telewizji. W zdecydowanej większości tego rodzaju oczekiwania pacjenta mają później negatywny przejaw w niezadowoleniu z efektu zabiegu, co wywołuje zniechęcenie oraz brak satysfakcji z osiągniętych celów. Jak podaje Barona, tego rodzaju zachowania w zdecydowanej większości dotyczą osób z niepełną edukacją, które często nie koncentrują się na przedyskutowaniu z lekarzem możliwego do osiągnięcia efektu zabiegu, okresu rekonwalescencji i postępowania w trakcie niej, ale trzymają się własnych, zbyt wygórowanych oczekiwań i wyobrażeń.
Jednak jak wskazują dane ASAPS, w 2014 roku w porównaniu do 2013 zostało wykonanych blisko o 7% mniej zabiegów (łączna wartość zarówno z zakresu chirurgii plastycznej, medycyny estetycznej oraz kosmetologii – 10.663.607).
W związku z danymi napływającymi zza oceanu nasuwa się pytanie, czy na świecie powoli zaczyna tworzyć się trend na naturalne piękno oraz nieinwazyjne metody odmładzania w odniesieniu do spadku popularności chirurgii plastycznej? Czy może sumaryczny spadek liczby wszystkich wykonanych procedur za 2014 rok jest skutkiem kryzysu gospodarczego oraz niepewnych czasów? Przyczyniać by się to mogło do tego, że rynek usług luksusowych, do których zalicza się medycynę estetyczną oraz kosmetologię, może zacząć przeżywać regres zainteresowania z korzyścią dla stosowania domowych sposobów zapobiegania efektom starzenia się skóry, w tym zdrowego stylu życia oraz większego nacisku na stosowanie preparatów przeciwstarzeniowych w kosmetykach do codziennej pielęgnacji skóry.
W badaniach ankietowych opublikowanych w 2014 roku w czasopiśmie naukowym „Handel wewnętrzny” na grupie 162 mieszkańców Trójmiasta, dla 55% zabiegi z zakresu medycyny estetycznej oraz kosmetologii były postrzegane jako zbyt drogie i luksusowe, natomiast 22% badanych uznało, że są one w przystępnej cenie. Badania przeprowadzono na przełomie 2013/2014 roku. Wówczas osoby które zadeklarowały, że korzystały z tego typu zabiegów przyznały, że najczęściej był to:
- botoks (33%),
- wypełniacze na bazie kwasu hialuronowego (29%),
- powiększanie ust (11%),
- mezoterapia (11%).
 Z kolei w raporcie "Rynek usług kosmetycznych w Polsce” wskazuje się na rozwój w kierunku funkcjonowania coachów zdrowia i stylu życia w duchu wellness. Jest to trend w Polsce dopiero rozpoczynający swoją karierę, który przybył zza oceanu i tam odnósł olbrzymi sukces. Osoby zajmujące się tym zawodowo miałyby oferować swoje usługi głównie w obiektach uzdrowiskowych, do których goście przyjeżdżają na dłuższy pobyt. Trenerzy pracują nad wprowadzeniem zmian w stylu życia, co miałoby odnieść długofalowe skutki w utrzymaniu zdrowia oraz dobrego samopoczucia. W USA, jak wynika z raportu, pakiety coachingowe obejmują również konsultację telefoniczną, mailową oraz przez skype’a. Rozwój w tym kierunku może świadczyć o tym, czego obecnie ludzie zaczynają oczekiwać od obiektów SPA oraz gabinetów medycyny estetycznej i kosmetologicznych - czy tylko holistyczne podejście, czy może moda na małą inwazyjność zabiegów z naciskiem na to jak żyjemy?
Z kolei w raporcie "Rynek usług kosmetycznych w Polsce” wskazuje się na rozwój w kierunku funkcjonowania coachów zdrowia i stylu życia w duchu wellness. Jest to trend w Polsce dopiero rozpoczynający swoją karierę, który przybył zza oceanu i tam odnósł olbrzymi sukces. Osoby zajmujące się tym zawodowo miałyby oferować swoje usługi głównie w obiektach uzdrowiskowych, do których goście przyjeżdżają na dłuższy pobyt. Trenerzy pracują nad wprowadzeniem zmian w stylu życia, co miałoby odnieść długofalowe skutki w utrzymaniu zdrowia oraz dobrego samopoczucia. W USA, jak wynika z raportu, pakiety coachingowe obejmują również konsultację telefoniczną, mailową oraz przez skype’a. Rozwój w tym kierunku może świadczyć o tym, czego obecnie ludzie zaczynają oczekiwać od obiektów SPA oraz gabinetów medycyny estetycznej i kosmetologicznych - czy tylko holistyczne podejście, czy może moda na małą inwazyjność zabiegów z naciskiem na to jak żyjemy?
Czy czytają to jacyś panowie? Jeśli tak, to na koniec coś o Was. Do niedawna panowała moda na metroseksualnych mężczyzn dbających o siebie niekiedy bardziej aniżeli część kobiet, korzystających z drobnych zabiegów kosmetycznych oraz chętnie sięgających po te ze świata medycyny estetycznej czy chirurgii plastycznej. Jak kiedyś modnym wśród panów było stosowanie botoksu, wypełniaczy czy poprawa urody u chirurga plastycznego, tak obecnie coraz więcej mówi się o nowym zjawisku. Jak podał z końcem ubiegłego roku "The Guardian", "Daily Mail", a także "Cosmopolitan", modnym zaczyna być mężczyzna lumberseksualny, inaczej drwal.
A jakie jest Wasze zdanie w tym temacie? Czy szykują się rewolucje w branży estetycznej? Zamieszczajcie swoje spostrzeżenia i ewentualne pytania lub uwagi pod artykułem.
Agnieszka Zabiegała,
stażystka portalu Biotechnologia.pl
dział: kosmetologia
Źródło: http://biotechnologia.pl/





















 Chłodziarka medyczna (cooler) Koolio jest niestymulującym urządzeniem do miejscowego schładzania skóry, które:
Chłodziarka medyczna (cooler) Koolio jest niestymulującym urządzeniem do miejscowego schładzania skóry, które:
 Wymiana wiadomości e-mail jest najbardziej rozpowszechnioną formą komunikacji w sieci. Jak wskazują badania obecnie aż 97% polskich internautów korzysta z poczty elektronicznej (IAB Polska, „Raport strategiczny Internet 2014”). E-mail to również niezwykle efektywne narzędzie do promocji usług salonu fryzjerskiego czy kosmetycznego.
Wymiana wiadomości e-mail jest najbardziej rozpowszechnioną formą komunikacji w sieci. Jak wskazują badania obecnie aż 97% polskich internautów korzysta z poczty elektronicznej (IAB Polska, „Raport strategiczny Internet 2014”). E-mail to również niezwykle efektywne narzędzie do promocji usług salonu fryzjerskiego czy kosmetycznego.
 Sprzęt dostępny od ręki, zapraszamy na próbny pokaz/zabieg do naszego centrum pokazowo - szkoleniowego.
Sprzęt dostępny od ręki, zapraszamy na próbny pokaz/zabieg do naszego centrum pokazowo - szkoleniowego.
 Sprzęt dostępny od ręki, zapraszamy na próbny pokaz/zabieg do naszego centrum pokazowo - szkoleniowego.
Sprzęt dostępny od ręki, zapraszamy na próbny pokaz/zabieg do naszego centrum pokazowo - szkoleniowego.
 W październikowym "Journal of Cosmetic Dermatology" ukazały się badania poświęcone temu, jakie cechy decydują o atrakcyjności kobiecych twarzy oraz jakie metody zapobiegania starzeniu się skóry zostały przyjęte lub są rozważane przez francuskie kobiety, aby zminimalizować niekorzystne oddziaływanie upływającego czasu na skórę twarzy. Okazuje się, że za główne wyznaczniki piękna i atrakcyjności ankietowane uznają: naturalny wygląd, pewność siebie oraz atrakcyjną, zadbaną skórę.
W październikowym "Journal of Cosmetic Dermatology" ukazały się badania poświęcone temu, jakie cechy decydują o atrakcyjności kobiecych twarzy oraz jakie metody zapobiegania starzeniu się skóry zostały przyjęte lub są rozważane przez francuskie kobiety, aby zminimalizować niekorzystne oddziaływanie upływającego czasu na skórę twarzy. Okazuje się, że za główne wyznaczniki piękna i atrakcyjności ankietowane uznają: naturalny wygląd, pewność siebie oraz atrakcyjną, zadbaną skórę. Niespodzianką wydaje się deklarowany negatywny stosunek do procedur z toksyną botulinową wyrażony przez blisko 92% ankietowanych. Zaledwie 1% przyznało, że korzystało z tego zabiegu przynajmniej jeden raz w życiu. Zaskoczenie jest o tyle duże, że według najnowszych doniesień ASAPS (American Society for Aesthetic Plastic Surgery) opublikowanych w odniesieniu do roku 2014 to właśnie toksyna botulinowa (Botox, Dysport, Xaomin) była najchętniej wykorzystywanym zabiegiem z niechirurgicznych procedur kosmetycznych w USA, zostawiając pilingi chemiczne dopiero na czwartym miejscu. Porównując jednak wartości procentowe z 2014 roku w odniesieniu do ilości zabiegów w roku 2013, interesującym w tym kontekście jest fakt, że ilość zabiegów z wykorzystaniem toksyny botulinowej w USA spadła o 4,7%, natomiast ilość procedur z wykorzystaniem pilingów chemicznych wzrosła o 9%.
Niespodzianką wydaje się deklarowany negatywny stosunek do procedur z toksyną botulinową wyrażony przez blisko 92% ankietowanych. Zaledwie 1% przyznało, że korzystało z tego zabiegu przynajmniej jeden raz w życiu. Zaskoczenie jest o tyle duże, że według najnowszych doniesień ASAPS (American Society for Aesthetic Plastic Surgery) opublikowanych w odniesieniu do roku 2014 to właśnie toksyna botulinowa (Botox, Dysport, Xaomin) była najchętniej wykorzystywanym zabiegiem z niechirurgicznych procedur kosmetycznych w USA, zostawiając pilingi chemiczne dopiero na czwartym miejscu. Porównując jednak wartości procentowe z 2014 roku w odniesieniu do ilości zabiegów w roku 2013, interesującym w tym kontekście jest fakt, że ilość zabiegów z wykorzystaniem toksyny botulinowej w USA spadła o 4,7%, natomiast ilość procedur z wykorzystaniem pilingów chemicznych wzrosła o 9%. Tab.1. Tabela opracowana na podstawie danych uzyskanych z raportu ASAPS (American Society for Aesthetic Plastic Surgery) z 2014r.
Tab.1. Tabela opracowana na podstawie danych uzyskanych z raportu ASAPS (American Society for Aesthetic Plastic Surgery) z 2014r. Z kolei w raporcie "Rynek usług kosmetycznych w Polsce” wskazuje się na rozwój w kierunku funkcjonowania coachów zdrowia i stylu życia w duchu wellness. Jest to trend w Polsce dopiero rozpoczynający swoją karierę, który przybył zza oceanu i tam odnósł olbrzymi sukces. Osoby zajmujące się tym zawodowo miałyby oferować swoje usługi głównie w obiektach uzdrowiskowych, do których goście przyjeżdżają na dłuższy pobyt. Trenerzy pracują nad wprowadzeniem zmian w stylu życia, co miałoby odnieść długofalowe skutki w utrzymaniu zdrowia oraz dobrego samopoczucia. W USA, jak wynika z raportu, pakiety coachingowe obejmują również konsultację telefoniczną, mailową oraz przez skype’a. Rozwój w tym kierunku może świadczyć o tym, czego obecnie ludzie zaczynają oczekiwać od obiektów SPA oraz gabinetów medycyny estetycznej i kosmetologicznych - czy tylko holistyczne podejście, czy może moda na małą inwazyjność zabiegów z naciskiem na to jak żyjemy?
Z kolei w raporcie "Rynek usług kosmetycznych w Polsce” wskazuje się na rozwój w kierunku funkcjonowania coachów zdrowia i stylu życia w duchu wellness. Jest to trend w Polsce dopiero rozpoczynający swoją karierę, który przybył zza oceanu i tam odnósł olbrzymi sukces. Osoby zajmujące się tym zawodowo miałyby oferować swoje usługi głównie w obiektach uzdrowiskowych, do których goście przyjeżdżają na dłuższy pobyt. Trenerzy pracują nad wprowadzeniem zmian w stylu życia, co miałoby odnieść długofalowe skutki w utrzymaniu zdrowia oraz dobrego samopoczucia. W USA, jak wynika z raportu, pakiety coachingowe obejmują również konsultację telefoniczną, mailową oraz przez skype’a. Rozwój w tym kierunku może świadczyć o tym, czego obecnie ludzie zaczynają oczekiwać od obiektów SPA oraz gabinetów medycyny estetycznej i kosmetologicznych - czy tylko holistyczne podejście, czy może moda na małą inwazyjność zabiegów z naciskiem na to jak żyjemy?
 Kombucza ma wiele synonimów – grzyb herbaciany, grzybek japoński czy szampan życia. Przypisuje mu się wiele właściwości zdrowotnych, ale badacze nie są zgodni co do bezpieczeństwa jego stosowania. To prawdziwy hit czy może kolejne oszustwo?
Kombucza ma wiele synonimów – grzyb herbaciany, grzybek japoński czy szampan życia. Przypisuje mu się wiele właściwości zdrowotnych, ale badacze nie są zgodni co do bezpieczeństwa jego stosowania. To prawdziwy hit czy może kolejne oszustwo? Nazwa wywodzi się prawdopodobnie od japońskich słów „kombu” (brązowa alga) i „cha” (napój). Grzyb herbaciany to prawdziwe bogactwo antyutleniaczy, witamin z grupy B, kwasów organicznych i wielu innych. Przypisuje mu się w związku z powyższym właściwości usprawniające trawienie (obecność dobroczynnych bakterii), oczyszczające organizm z toksyn, usprawniające metabolizm, immunostymulujące a nawet antynowotworowe. Kombucza ma również obniżać ciśnienie krwi, regulować poziom cholesterolu, łagodzić bóle migrenowe, poprawiać jakość widzenia, przyspieszać gojenie ran a nawet... spowalniać siwienie włosów. Można rzec po przeczytaniu „litanii” hiperwłaściwośći, że doczekaliśmy się cudownego panaceum! I wszystko byłoby pięknie gdyby nie to, że badacze nie są zgodni co do bezpieczeństwa stosowania grzybka herbacianego...
Nazwa wywodzi się prawdopodobnie od japońskich słów „kombu” (brązowa alga) i „cha” (napój). Grzyb herbaciany to prawdziwe bogactwo antyutleniaczy, witamin z grupy B, kwasów organicznych i wielu innych. Przypisuje mu się w związku z powyższym właściwości usprawniające trawienie (obecność dobroczynnych bakterii), oczyszczające organizm z toksyn, usprawniające metabolizm, immunostymulujące a nawet antynowotworowe. Kombucza ma również obniżać ciśnienie krwi, regulować poziom cholesterolu, łagodzić bóle migrenowe, poprawiać jakość widzenia, przyspieszać gojenie ran a nawet... spowalniać siwienie włosów. Można rzec po przeczytaniu „litanii” hiperwłaściwośći, że doczekaliśmy się cudownego panaceum! I wszystko byłoby pięknie gdyby nie to, że badacze nie są zgodni co do bezpieczeństwa stosowania grzybka herbacianego...
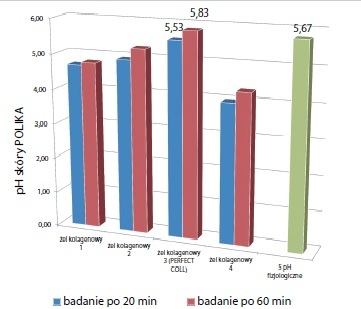
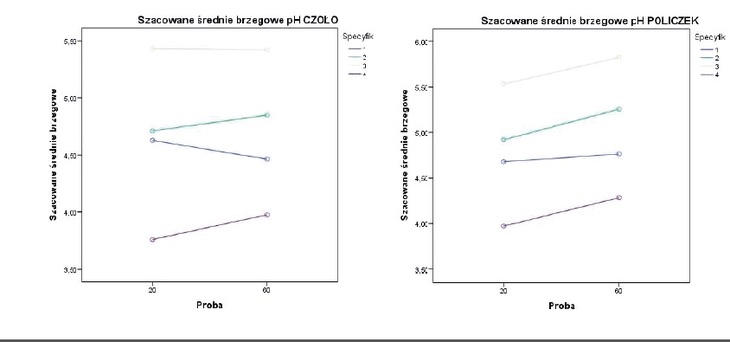
 Skóra to największy narząd naszego ciała, spełniający wiele kluczowych funkcji: ochroną, wydzielniczą i czuciową. Płaszcz hydro-lipidowy warstwy rogowej naskórka jest bardzo istotnym czynnikiem dla przepuszczalności bariery skórnej nie tylko pod względem ochrony przeciwbakteryjnej, ale również dla czynników fizjologicznych i patologicznych, które mogą zmieniać poziom zakwaszania.
Skóra to największy narząd naszego ciała, spełniający wiele kluczowych funkcji: ochroną, wydzielniczą i czuciową. Płaszcz hydro-lipidowy warstwy rogowej naskórka jest bardzo istotnym czynnikiem dla przepuszczalności bariery skórnej nie tylko pod względem ochrony przeciwbakteryjnej, ale również dla czynników fizjologicznych i patologicznych, które mogą zmieniać poziom zakwaszania.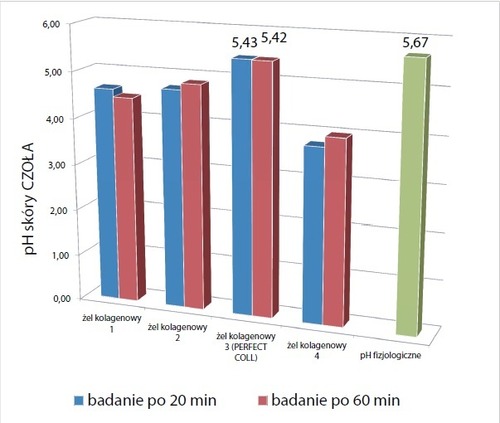

 W lutym w Warszawie odbędzie się kolejne szkolenie w ramach, zainicjowanej przez Versum, Akademii Zarządzania Salonami Urody. Tym razem spotkanie poprowadzi trener biznesu Marta Fiłoń.
W lutym w Warszawie odbędzie się kolejne szkolenie w ramach, zainicjowanej przez Versum, Akademii Zarządzania Salonami Urody. Tym razem spotkanie poprowadzi trener biznesu Marta Fiłoń.
 N-Renewal jest nową linią produktów do mezoterapii frakcyjnej opracowaną przez laboratorium N-Symbiosis Polska. Celem który przyświecał technologom była pomóc kobietom jak i mężczyznom, wyglądać młodziej i utrzymać swój dotychczasowy wygląd jak najdłużej. Preparaty nawilżają dojrzałą skórę, redukują zmarszczki powstrzymują objawy starzenia. Substancje aktywne i wspomagające w koktajlach N-Renewal są składnikami tkanek skóry. Z wiekiem zmniejszony metabolizm Naszego organizmu powoduje silne procesy starzenia. Z wiekiem naskórek staje się cieńszy , a w konsekwencji zmniejsza się bariera, która chroni skórę przed utratą wilgotności i przesuszaniem. Liczba komórek zmniejsza się o około 10 procent każdego roku, co uniemożliwia prawidłową regenerację skóry.
N-Renewal jest nową linią produktów do mezoterapii frakcyjnej opracowaną przez laboratorium N-Symbiosis Polska. Celem który przyświecał technologom była pomóc kobietom jak i mężczyznom, wyglądać młodziej i utrzymać swój dotychczasowy wygląd jak najdłużej. Preparaty nawilżają dojrzałą skórę, redukują zmarszczki powstrzymują objawy starzenia. Substancje aktywne i wspomagające w koktajlach N-Renewal są składnikami tkanek skóry. Z wiekiem zmniejszony metabolizm Naszego organizmu powoduje silne procesy starzenia. Z wiekiem naskórek staje się cieńszy , a w konsekwencji zmniejsza się bariera, która chroni skórę przed utratą wilgotności i przesuszaniem. Liczba komórek zmniejsza się o około 10 procent każdego roku, co uniemożliwia prawidłową regenerację skóry.
 Z wiekiem skóra każdego z nas starzeje się. Pojawiają się zmarszczki, zwiotczenia i przebarwienia, naskórek jest ścieńczały. Spada aktywność fibroblastów i zmniejsza się ilości włókien kolagenowych i elastanowych. Skóra regeneruje się zdecydowanie wolniej, ponieważ osłabieniu ulegają jej mechanizmy obronne. Procesy różnicowania się komórek spowalniają. Obniżona zostaje odporność na stres i czynniki środowiskowe. Zmniejsza się ilość glikozaminoglikanów i proteoglikanów. Melanina jest rozkładana nierównomiernie i zmniejsza się ilość gruczołów łojowych.
Z wiekiem skóra każdego z nas starzeje się. Pojawiają się zmarszczki, zwiotczenia i przebarwienia, naskórek jest ścieńczały. Spada aktywność fibroblastów i zmniejsza się ilości włókien kolagenowych i elastanowych. Skóra regeneruje się zdecydowanie wolniej, ponieważ osłabieniu ulegają jej mechanizmy obronne. Procesy różnicowania się komórek spowalniają. Obniżona zostaje odporność na stres i czynniki środowiskowe. Zmniejsza się ilość glikozaminoglikanów i proteoglikanów. Melanina jest rozkładana nierównomiernie i zmniejsza się ilość gruczołów łojowych.